کمی لومینسانس ایمنواسی
کمی لومینسانس ایمنواسی
و استفاده از آن در آزمایشگاه های تشخیص پزشکی
روش ایمنواسی اصولا به آزمایش هایی گفته می شود که بر اساس اتصال آنتی بادی و آنتی ژن بنا شده است. شاخه ای از این آزمایش ها را ایمنواسی بر پایه آنزیم[1] گویند که در آن آنزیم خاصی با آنتی بادی نشاندار (کونژوگه) می شود تا سیگنالی ( مانند رنگ یا نور) تولید کند که رابطه مستقیم یا غیر مستقیم با غلظت آنالیت درون نمونه داشته باشد. روش های ایمنواسی می تواند به چند دسته تقسیم شود،مانند: رادیوایمنواسی[2]، الایزا[3]، کمی لومینسانس ایمنواسی[4] و فلورسانس ایمنواسی[5]. تفاوت در اکثر این روش ها به مولکول نشاندار شده به آنتی بادی و نوع سیگنالی که تولید می کند بستگی دارد.
روش رادیوایمنواسی اولین بار در سال 1959 توسط دو دانشمند با نام های Yalow و Berson ابداع شد. آنها از 125I به عنوان نشانگر استفاده کردند. اگرچه تکنیک رادیوایمنواسی روشی قابل اطمینان، معتبر و دقیق بود اما رادیوایزوتوپ ها مشکلاتی از قبیل کوتاهی نیمه عمر و ایمنی را بوجود آورده بودند که امکان گسترش استفاده از آن را بسیار محدود کرده بود.
چند سال بعد دو دانشمند با نام های Engvall و Perlmann در سال 1971 روش الایزا را ابداع کردند. از آن پس این روش بطور گسترده در آزمایشگاه های تشخیص طبی، آسیب شناسی گیاهی و صنایع غذایی مورد استفاده قرار گرفت. با پیشرفت علم و نیاز آزمایشگاه ها به تشخیص آنالیت هایی با غلظت کمتر، سمت و سوی تحقیقات به ابداع روشی حساس تر، دقیق تر و سریعتر مانند فلورسانس و کمی لومینسانس رو آورد. در میان تکنینک های ایمنواسی، روش الایزا رشدی بسیار سریع داشت. استفاده از آن بسیار ایمنتر و آسانتر از رادیوایمنواسی بود. الایزا بر اساس رنگ تولید شده از واکنش آنزیم کونژوگه با سوبسترای آنزیمی می باشد. دانسیته این رنگ تولید شده بر اساس قانون بیرلامبرت و منحنی استاندارد به غلظت تبدیل می شود. به هر حال حساسیت روش الایزا که مبتنی بر کالریمتری مرسوم است نسبتا پایین بود. به همین منظور ایمنواسی برای گسترش و افزایش حساسیت نیازمند تغییرات گسترده تر شد.
در سال 1985 یک دانشمند بنام Woodhead روش کمی لومینانس ایمنواسی را ابداع نمود. درمیان روش های ایمنواسی، کمی لومینسانس ایمنواسی نماینده یک تکنیک چندکاره، فوق حساس با رنج وسیعی از کاربرد در آزمایشگاه ظهور کرد. امروزه این روش بعنوان پرکاربرد ترین نسل تکنولوژی برای تشخیص در حوزه علوم آزمایشگاهی است. در این تکنیک از یک ماده لومینسانس بعنوان نشانگر[6] استفاده می شود. CLIA این امکان را فراهم کرد تا زمان انجام واکنش کوتاه تر شود و شرکت های تولید کننده کیت های آزمایشگاهی بتوانند محصولات خود را در قالب یک سیستم بسته (Closed) بصورت یک کارتریج تولید کنند تا بسیاری از خطاهای انسانی حذف شود. CLIA باعث کاهش مدت زمان آزمایش از یک و نیم ساعت به 45-30 دقیقه شد.
اگرچه CLIA حساسیت ایمنواسی را بهبود بخشید، اما اتصال مستقیم نشانگرهای لومینسانس بخاطر کوتاهی مدت زمان نشر نور استفاده از آن را بصورت اتوماتیک محدود کرد. هرچه طول مدت تابش نور کمتر و سریعتر باشد، تمام انرژی برانگیختگی صرف تابش نور شده و فرصتی برای تبدیل نور به انرژی گرمایی و به هدر رفتن آن وجود ندارد. به همین دلیل چنانچه آزمایش به کمک ربات های تمام اتوماتیک و بصورت Closed انجام شود، خطاهای زمینه ای حذف شده و راندمان و بازدهی کار نسبت به روش دستی آن بسیار بیشتر خواهد بود.
CLIA جایگزین خوبی بجای RIA و ELISA برای تشخیص حساس و دقیق موادی مانند پروتئین، هورمون، دارو، اسیدهای نوکلئیک و آلوده کننده های محیط زیست است. در سال های اخیر، CLIA بعلت حساسیت بالا، گستردگی رنج و کامل شدن روش های اتوماسیون در حوضه بیوشیمی بالینی رشد فراوانی کرده است. CLIA با گسترش و کاربرد تکنولوژی آنتی بادی های نوترکیب، نشانگرها و تکنیک های وابسته، مواد فاز جامد و بهبود در عملکرد ربات ها، بعنوان روشی نوین ظهور کرد.
معرف ها برای انجام واکنش نیازبه نشانگرهایی دارند که به آنتی بادی و یا آنتی ژن های خاصی متصل شوند و فرایندی را باعث شوند که در نهایت به تولید نور بیانجامد. از جمله این نشانگرها که بیشترین استفاده را در کمی لومینسانس ایمنواسی دارند می توان به آنزیم فسفاتاز قلیایی[7]، لومینول، ایزولومینول و مشتقات آن، اکریدین استر و HRP[8] اشاره کرد. از مواد لومینسانسی که دارای پایین ترین محدوده قابل اندازه گیری[9] هستند می توان به روش های مبتنی بر آنزیم فسفاتاز قلیایی، لومینول، ایزولومینول و اکریدین استر اشاره کرد. امروزه بیشترین کیت های CLIA موجود در بازار جهانی منطبق بر آنزیم فسفاتاز قلیایی، ایزولومینول و اکریدین استر هستند. زیرا طبق مطالعات صورت گرفته بیشترین حساسیت، پایینترین LOD را دارند و برای سیستم های بسته CLIA بسیار مناسب هستند و از طرف دیگر پایدارتر از مابقی لومینانس ها می باشند و کاربری آن ها بسیار راحت تر از بقیه مواد لومینسانس می باشد.
اخیرأ روش هایی که از سیستم میکروذرات[10] مخصوصأ میکروذرات مغناطیسی بعنوان فاز جامد در ایمنواسی استفاده می شود توجه دانشمندان را به خود معطوف کرده است. از مزایای این میکروذرات میشود به امکان تولید آنها در اندازه های مختلف و با خصوصیات منحصر به فرد نام برد. همچنین بعلت اینکه این میکروذرات سازگاری خوبی با مواد زیستی دارند و از نظر اندازه با سایر مواد بیولوژیکی همخوانی مطلوبی دارند، به راحتی می توانند به آنتی بادی متصل شوند و عملکرد خوبی داشته باشند. میکروذرات مغناطیسی باعث افزایش سطح اتصال آنتی بادی یا آنتی ژن های اختصاصی در مقایسه با سطح محدود هر چاهک در روش ELISA میشود. از طرف دیگر معلق بودن میکروذرات در ماتریکس نمونه باعث افزایش احتمال واکنش با آنالیت مورد نظر می شود. همین امر باعث افزایش حساسیت، تکرارپذیری بالا، افزایش گستره محدوده خوانش، بهبود در کمترین میزان قابل اندازه گیری و کاهش زمان واکنش CLIA در مقایسه با روش های دیگر مانند ELISA میشود. همچنین محدوده خطی[11] بالاتری در رنج وسیع تری از آنالیت موجود در نمونه خواهد داشت و میتواند آنالیت هایی با کمترین مقدار را اندازه گیری کند. جداسازی کمپلکس آنتی بادی-آنتی ژن در روش CLIA بسیار آسانتر و سریعتر از روش ELISA می باشد. تنها کافیست محیط واکنش در یک میدان مغناطیسی قرار بگیرد تا مواد واکنشگر که اتصال اختصاصی نداشته اند شسته شود و فقط کمپلکس مورد نظر در کووت واکنش باقی بماند. همچنین میکروذرات پوشیده از آنتی بادی توانایی اتصال به آنالیت های کوچک قرار گرفته در محلولی با مولکول های بزرگ را نیز دارد.
|
|
|
|
|
|

شکل 1: میکروذرات پوشیده شده با مواد و زنجیره های جانبی مختلف
افزایش سطح اتصال آنتی بادی و افزایش احتمال تصادم مولکولهای واکنشگر یکی از عوامل مهم و تاثیرگذار در افزایش سرعت و بهبود عملکرد واکنش است. در سیستم های CLIA جدید مانند دستگاه INDRA200 که از میکروذرات مغناطیسی استفاده می شود، این افزایش در سطح میکروذرات مغناطیسی چندین برابر سطح چاهک میکروپلیت در روش ELISA شده است. همچنین معلق بودن میکروذرات مغناطیسی در محیط واکنش باعث افزایش احتمال واکنش آنتی بادی با آنتی ژن می شود. این عوامل باعث افزایش سرعت و عملکرد در سیستم های بسته CLIA در مقایسه با روش الایزا شده است. اندازه قابل تنظیم انتشار نور، طیف انتشار باریک، طیف تحریک گسترده و نقاط کوانتومی لومینسانس بسیار[12]، در سیستم های CLIA توجه دانشمندان را بطور شگرف بخود جذب کرد تا از این سیستم بعنوان یک روش حساس، دقیق و پرسرعت جهت گسترش علم تشخیص در آزمایشگاه های پاتوبیولوژی و تشخیص پزشکی استفاده کنند.
در روش الایزا برای جداسازی آنتی بادی متصل شده به آنالیت باید سطح داخلی چاهک های پلیت با آنتی بادی پوشیده شود که این اتصال مستقیم آنتی بادی با سطح پلی استایرنی پلیت الایزا میتواند اثرات نامطلوبی مانند عدم تکرارپذیری، کاهش حساسیت و افزایش قیمت بدلیل استفاده از غلظت های بالاتری از مواد بیولوژیک در آزمایش بگذارد. اما این نقصان در روش CLIA با گسترش علم میکروذرات مغناطیسی و استفاده از موادی مانند بیوتین-استرپتاویدین مرتفع گردیده است. آنتی بادی اختصاصی بر روی سطح میکروذرات مغناطیسی پوشیده می شود (کووت[13] می شود) که با قرارگیری کووت در میدان مغناطیسی مطلوب با قدرت مشخص کمپلکس تشکیل شده میکروذرات با آنالیت هدف در چاهک باقی میماند و بقیه محلولها توسط سیستم شسته میشوند. در این حالت دیگر نیازی به پوشیدن سطح داخلی چاهک نمیباشد.

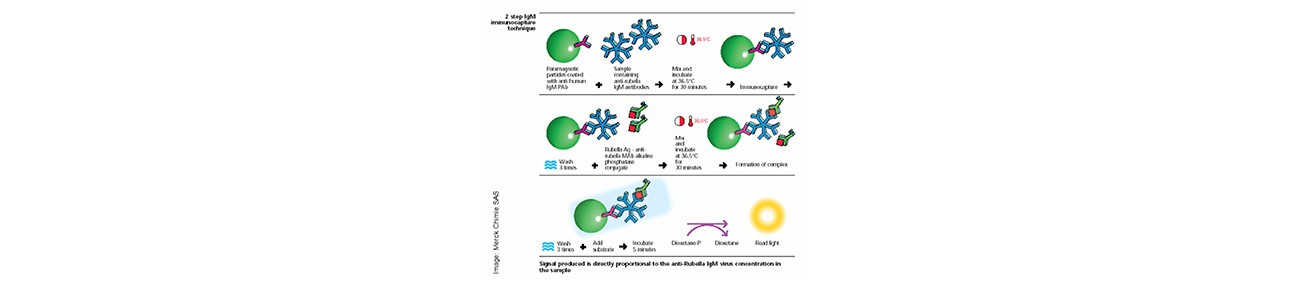
شکل 2: طرح شماتیک یک روش اندازه گیری آنتی بادی IgM به روش کمی لومینسانس ایمنواسی
خصوصیات میکروبید های مغناطیسی استفاده شده در کیت های تجاری بسیار متنوع هستند. اندازه هر مگنتیک میکروبید تاثیر مستقیم در سیستم جداسازی کمپلکس و همچنین سرعت رسوب در میدان مغناطیسی دارد. گروه های عاملی پوشیده شده در سطح میکروبیدهای مغناطیسی قدرت سیگنال تولید شده را در کیت های تجاری تعیین می کنند. هرچه سیگنال بوجود آمده بالاتر باشد احتمال خطا در خوانش و تکرارپذیری کمتر خواهد بود. مقدار یون آهن استفاده شده در این میکروبیدها سرعت جداسازی فاز جامد از مایع را مشخص می کنند. اتصال گروه های عاملی به زنجیره های آمین یا کربوکسیل آنتی بادی و آنتی ژن، ثابت اتصال و جداسازی آن ها و نیز پایداری اتصال شکل گرفته در سطح میکروبیدهای مغناطیسی تاثیر بسزایی در عملکرد روش های بسته مبتنی بر تکنولوژی مگنتیک میکروبید و کمی لومینسانس دارند.
سیستم های بسته ربات های تمام خودکار در روش کمی لومینسانس عملکرد بسیار بهتری در مقایسه با روش های دیگر اندازه گیری مواد بیولوژیک دارند. استفاده از سیستم جداسازی میکروبیدهای مغناطیسی و نشانگر های کمی لومینسانس شاخص های عملکردی آزمایش را در مقایسه با روش های دیگر مانند الایزا تا حد چشمگیری افزایش داده است.

شکل 3: مقایسه روش های مختلف بر اساس توانایی آن ها در اندازه گیری انالیت هدف
بطور کلی روش کمیلومینسانس ایمنواسی (CLIA) با بهرهگیری از نشانگرهای مناسب برای ردیابی آنتی ژن، میکروذرات مغناطیسی برای افزایش سطح و جداسازی آنتی ژن با سرعت و حساسیت و دقت بالا، استفاده از آنتی بادی های منوکلونال و سیستم های خوانشگر دقیق (PMT[14]) که باعث افزایش حساسیت، محدوده خطی بیشتر (بعضأ تا 4 برابر فتومترهای الایزا)، افزایش تکرارپذیری، افزایش سرعت انجام واکنش، بهبود در کمترین حد خوانش (LOD)، کالیبراسیون مناسب با ضریب همبستگی بهتر و شیب خطی بالاتر که نشان دهنده حساسیت و دقت بیشتری در مقایسه با الایزا است، همبستگی خطی بهتر در رقت های متوالی، احتمال وجود اثر هوک[15] در غلظتهای بسیار بالاتر در مقایسه با روش الایزا، کاهش مقدار نمونه مورد آزمایش، کاهش مدت زمان انجام واکنش، کاهش زمان پاسخگویی به بیمار و اطمینان به جواب های آزمایش بعنوان یک جایگزین مطمئن برای روش الایزا می باشد.
نویسنده: دکتر میلاد دولتخواه (مسئول فنی شرکت آپادانا تابناک سیستم)
[1] Enzyme immunoassay (EIA)
[2] Radioimmunoassay (RIA)
[3] Enzyme-linked immunosorbent assay (ELISA)
[4] Chemiluminescence immunoassay (CLIA)
[5] Fluorescence Immunoassay (FIA)
[6] Label
[7] Alkaline Phosphatase (ALP)
[8] Horseradish Peroxidase (HRP)
[9] Limit of Detection (LOD)
[10] Microparticles
[11] Linearity
[12] Quantum Dots (QDs)
[13] Coat
[14] Photomultiplier tubes
[15] Hook Effect

